
Back كلوريد السلفوريل Arabic سولفوریل کولورید AZB Sulfurylchlorid German Sulfuryl chloride English Sulfurila klorido Esperanto Cloruro de sulfurilo Spanish سولفوریل کلرید Persian Sulfuryylikloridi Finnish Chlorure de sulfuryle French सल्फ्यूराइल क्लोराइड Hindi
| Chlorid sulfurylu | |
|---|---|
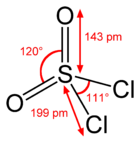 Struktura molekuly chloridu sulfurylu | |
 Kapalná forma | |
| Obecné | |
| Systematický název | chlorid sulfurylu |
| Ostatní názvy | sulfurylchlorid dichlorid-dioxid sírový |
| Anglický název | Sulfuryl chloride |
| Německý název | Sulfurylchlorid |
| Sumární vzorec | SO2Cl2 |
| Vzhled | bezbarvá kapalina (postupem času žloutnoucí) |
| Identifikace | |
| Registrační číslo CAS | 7791-25-5 |
| EC-no (EINECS/ELINCS/NLP) | 232-245-6 |
| Indexové číslo | 016-016-00-6 |
| Vlastnosti | |
| Molární hmotnost | 134,971 g/mol |
| Teplota tání | −54,1 °C |
| Teplota varu | 69,1 °C |
| Teplota rozkladu | 160 °C |
| Hustota | 1,709 1 g/cm3 (0 °C) 1,66 g/cm3 (20 °C) 1,657 0 g/cm3 (25 °C) |
| Index lomu | nD= 1,443 7 |
| Rozpustnost ve vodě | reaguje |
| Rozpustnost v polárních rozpouštědlech | aceton |
| Rozpustnost v nepolárních rozpouštědlech | kapalné uhlovodíky chlorované uhlovodíky sirouhlík |
| Relativní permitivita εr | 9,15 (22 °C) |
| Tlak páry | 5,45 kPa (0 °C) 12,69 kPa (18 °C) 33,61 kPa (39 °C) 51,41 kPa (50 °C) |
| Měrná magnetická susceptibilita | −5,08×10−6 cm3g−1 |
| Struktura | |
| Tvar molekuly | tetraedr |
| Dipólový moment | 6,0×10−30 Cm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −389,8 kJ/mol |
| Entalpie varu ΔHv | 208 J/g |
| Standardní molární entropie S° | 216,3 JK−1mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | −305,0 kJ/mol |
| Izobarické měrné teplo cp | 0,973 5 JK−1g−1 |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H314 H335 EUH014 |
| R-věty | R14 R34 R37 |
| S-věty | (S1/2) S26 S45 |
Některá data mohou pocházet z datové položky. | |
Chlorid sulfurylu (též sulfurylchlorid) (SO2Cl2) je sloučenina síry, kyslíku a chloru. Při pokojové teplotě je to bezbarvá kapalina štiplavého zápachu. Chlorid sulfurylu se nevyskytuje v přírodě, což lze dovodit i z toho, že podléhá rychlé hydrolýze.
Chlorid sulfurylu bývá často zaměňován s chloridem thionylu, SOCl2. Vlastnosti obou oxychloridů síry jsou však podstatně odlišné: chlorid sulfurylu je zdrojem chloru, kdežto chlorid thionylu je zdrojem chloridových iontů.
- ↑ a b Sulfuryl chloride. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)

